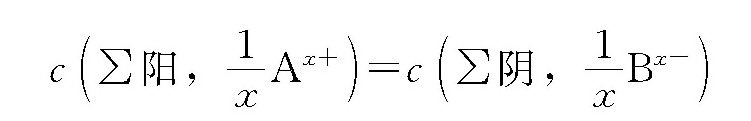硅酸化合物也是天然水中的一种主要杂质,研究其形态,对于制备除盐水是至关重要的。硅酸化合物存在的形态,与水的性质有关,特别是水的pH值对其影响很大。由于pH值变化,其形态也很多,也比较复杂。硅酸可以写成通式xSiO2·yH2O。在水中存在形态为:
当x=1,y=1时,成为偏硅酸H2SiO3;
当x=1,y=2时,成为正硅酸H4SiO4;
当x>1时,成为多硅酸,如H2Si2O5等。
这些硅酸在水中的溶解度极小。从其溶度积可知(25℃时,H2SiO3溶度积为1×10-11),当pH值等于6时,其溶解度只有0.005mmol/L,当pH等于7时,为0.05mmol/L。由此可知:硅酸在酸性或微酸性的水溶液中,很少以离子态存在,pH值越低,离子态的硅酸化合物越少,而胶体硅却越多。只有pH值大于10.5时,才有少量的SiO2-3存在。总之,在天然水中,硅酸呈溶解状态和胶体硅两种形式,不同形式硅酸的比例与水的氢离子浓度即pH值有关。
离子交换除盐处理,只能除去水中溶解状的硅酸化合物,胶体硅大都是通过混凝澄清处理予以去除。而用钼蓝法测定水中硅酸化合物时,也只能测定溶解状硅酸化合物。而全硅量的测定,要事先将胶体硅用氢氟酸转化成溶解状硅酸化合物,然后,再用钼蓝法测定。