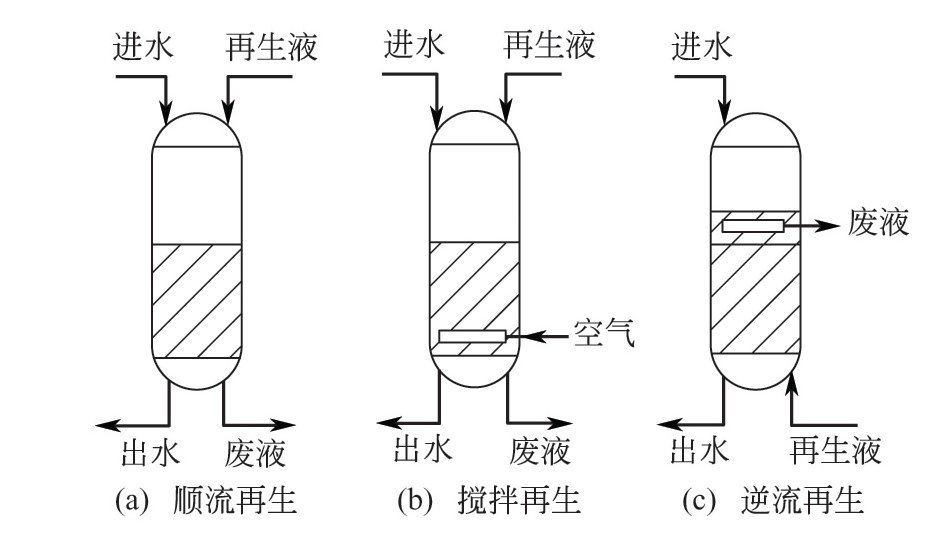
离子交换剂和水中离子之间的离子交换反应是可逆的,并按等电荷摩尔量进行。它们之间的离子交换根据质量作用定律,当正反应速度和逆反应速度相等的时候,溶液中各种离子的浓度就不再改变而达到平衡,即称为离子交换平衡。
离子交换反应的通式为:
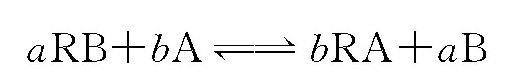
式中 a、b———A、B离子的价数,则平衡常数的通式为:
例如H型强酸性阳离子交换树脂RH,同水中Na+进行交换,其反应式如下:
按照质量作用定律,在离子交换反应达到平衡时,树脂中含Na+浓度和H+浓度的比值[RNa]/[RH],与水中Na+浓度与H+浓度的比值[Na+]/[H+]成正比关系。其比值在一定的温度条件下是一个常数,称为平衡常数或离子交换选择性系数,以K表示:
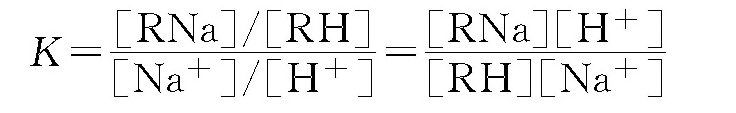
式中 K———离子交换平衡常数;
[RNa]———反应平衡时交换剂中Na+浓度,mol/L;
[RH]———反应平衡时交换剂中H+浓度,mol/L;
[H+]———反应平衡时水溶液中H+浓度,mol/L;
[Na+]———反应平衡时水溶液中Na+浓度,mol/L。
从平衡常数K的大小,可以看出交换剂上的H+变成Na+的难易程度。如果K>1,则Na+容易到交换剂上去,而把H+放出来,K越大,就越容易吸附Na+而放出H+。对于一定的树脂来说,与水中不同的离子,有不同的交换能力。因此,K值的大小各不相同。如H型强酸性阳离子交换树脂,对水中常见的几种阳离子的平衡常数K如下:

Na型强酸性阳离子交换树脂对水中几种阳离子的平衡常数K如下:

OH型强碱性阴离子交换树脂(Ⅰ型)对水中常见的几种阴离子的交换平衡常数K如下:

Cl型强碱性阴离子交换树脂(Ⅰ型)对水中几种阴离子的平衡常数K如下: