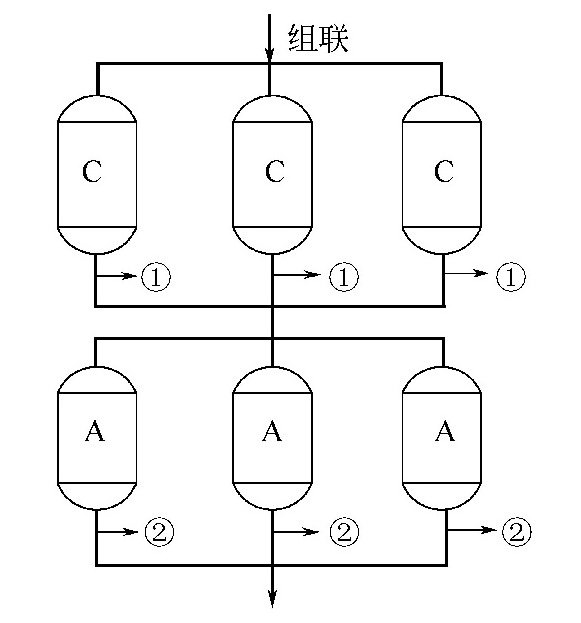
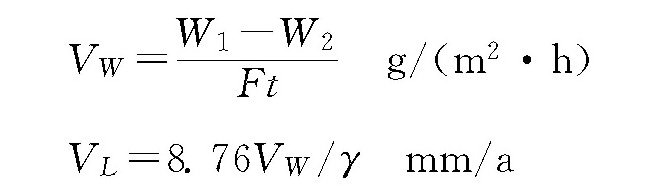金属腐蚀过程中,电流在阳极部位和阴极部位间流动,这说明阳极部位和阴极部位间有电位差。如果水中不含氧,阳极腐蚀反应的电子在阴极发生以下反应:2e+2H→+2H→H2
生成的原子态氢和氢气覆盖在阴极表面,产生了与腐蚀电位相反的电压,称为氢气的超电压,使电位差起了变化,阻止了电流的流动,也就是停止了腐蚀过程的进行。这种由于反应生成物所引起的电位差变化称为极化。氢气在腐蚀过程中起了极化作用,极化作用起了抑制腐蚀过程的作用。
当水中有溶解氧存在时,阴极反应按下式进行:
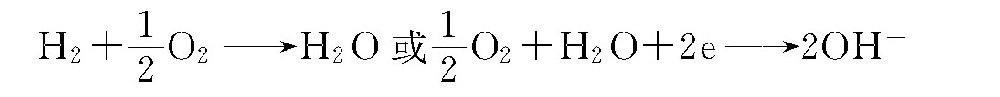
由于氧参加了反应,夺走了覆盖在阴极表面上的原子态氢和氢气,因而使氢气的极化作用遭到破坏。排除极化的作用称为去极化,氧在腐蚀过程中起了去极化作用,去极化作用起了助长腐蚀过程的作用。